lityum hakkında bilgi nedir tdk sözlük anlamı ne?
isim, kimya, (li'tyum), Fransızca lithiumAtom numarası 3, atom ağırlığı 6,94, yoğunluğu 0,55 olan, 180 °C'de eriyen, gümüş parlaklığında, bilinen en hafif element (simgesi Li).
lityum (Kimya Terimleri Sözlüğü (II) - 2007)
İngilizce: Lithium, Fransızca: lithium, Almanca: Lithium
Simgesi Li, atomik kütlesi 6,941 g, atom numarası 3, yoğunluğu 0,524 g/mL, e.n. 180 °C, k.n. 1340 °C olan çok az miktarda Al’un sertliğini artıran, tuzları sabunlarda, yağlayıcılarda ve tıpta kullanılan periyodik çizelgede 1. grubtaki ilk alkali metal olan ve küçük miktarlarda geniş yayılımı olan gümüş renginde bir metal.
Lityum Kelimesinin Kökeni
Yeni Latince lithium "metalik bir element" sözcüğünden alıntıdır. (İlk kullanımı: 1808 Jöns Jakob Berzelius İsv. kimyacı.) Latince sözcük Latince lithia "lityum oksit minerali" sözcüğünden türetilmiştir. Bu sözcük Eski Yunanca líthos λίθος "taş" sözcüğünden türetilmiştir.
Lityum Kelimesi için Tarihteki En Eski Kaynak
[TDK, Türkçe Sözlük, 1. Baskı (1945)]
Lityum (Li)
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Temel özellikleri
 |
| Lityumun görünüşü: Gümüşümsü beyaz, gri |
Atom numarası: 3
Element serisi: Alkali metaller
Grup, periyot, blok: 1, 2, s
Atom ağırlığı: 6.941(2) g/mol g/mol
Elektron dizilimi: 1s22s1
Enerji seviyesi başına Elektronlar: 2,1
CAS kayıt numarası: 7439-93-2
Lityumun Fiziksel Özellikleri
Maddenin hâli: Katı
Yoğunluk: 0.534 g·cm−3 g/cm³
Sıvı hâldeki yoğunluğu: 0.512 g·cm−3 g/cm³
Ergime noktası: 453.69 °K - 180.54 °C
Kaynama noktası: 1615 °K - 1342 °C
Ergime ısısı: 3.00 kJ/mol
Buharlaşma ısısı: 147.1 kJ/mol
Isı kapasitesi: 24.860 J/(mol·K)
Lityumun Atom özellikleri
Kristal yapısı: kübik yüzey merkezli
Yükseltgenme seviyeleri: 1
Elektronegatifliği: 0,98 Pauling ölçeği
İyonlaşma enerjisi: 1.seviye: 520.2 - 2.seviye: 7298.1 - 3.seviye: 11815.0 kJ/mol
Atom yarıçapı: 145 pm
Atom yarıçapı (hes.): 167 pm
Kovalent yarıçapı: 134 pm
Van der Waals yarıçapı: 182 pm
Diğer özellikleri
Elektrik direnci: 92,8 nΩ·m (20°C'de)
Isıl iletkenlik: 84,8 W/(m·K)
Isıl genleşme: 46 µm/(m·K) (25°C'de)
Ses hızı: 6000 m/s ('de)
Mohs sertliği: 0,6
Vickers sertliği: MPa
Brinell sertliği: MPa
Genel özellikleri
Birinci grup elementi olmasına rağmen,lityum aynı zamanda 2. grubun toprak alkali özelliklerini de gösterir. Bütün alkali metaller gibi bir tane değerlik elektronu bulunur ve bu elektronu hemen kaybederek pozitif iyon haline geçer. Bu sebeplerden dolayı lityum su ile çok kısa sürede reaksiyona girer ve doğada doğal halinde bulunmaz. Ancak kendisiyle benzer kimyasal özellikler taşıyan sodyum elementi lityuma göre daha aktiftir ve daha çok insanların midelerinde yer alır
Lityum bıçakla kesilebilinir, sodyumdan biraz daha sert olduğu için, onu kesmek veya bölmek çok daha zordur. Reaksiyona girmemiş Lityum gümüşi bir renge sahiptir, ancak kısa sürede rengi kararır. Düşük yoğunluğu sayesinde hidrokarbonlar üzerinde batmadan durabilir.
Alev üzerine konulduğunda lityumda göz alıcı bir kırmızı renk gözlenir, ancak yanmaya başladığında parlak beyaz bir alev gözlemlenir. Lityum suda ve su buharında bulunan oksijen ile tutuşur ve yanma reaksiyonu gösterir. Oda sıcaklığında azot ile reaksiyona giren tek metaldir. Yüksek özgül ısısı, 3582 J/(kg·K), ve sıvı haldeki geniş sıcaklık değerleri lityumu kullanışlı hale getirmektedir.
Lityum hava ve su ile yanması ve potansiyel patlama tehlikesine rağmen diğer alkali metallere göre daha az tehlikelidir. Oda sıcaklığındaki Lityum-Su reaksiyonu aktif ve çabuk gerçekleşen bir reaksiyon olmasına rağmen çok tehlikeli bir reaksiyon değildir. Lityum alevlerini söndürmek zordur ve bunun için özel kimyasallardan oluşan söndürücüler kullanılır.
Lityum, ten ile temasını engellemek için özel koruma gerektirir. Lityumu toz olarak ya da alkalinli bileşimlerinin solunması, burun yollarında ve boğaz da tahriş ve zarara neden olur.
Tarihçe
Lityum ilk olarak 1817 yılında Johan August Arfwedson tarafından keşfedilmiştir. İlk saf olarak izolasyonu ise William Thomas Brande ve Humphrey Davy tarafından lityum oksitten elektroliz yolu ile gerçekleştirilmiştir. Spodumen cevheri ,LiAl(SiO3)2, Lityum içeriği nedeniyle ticarı olarak çok önemlidir. Öncelikle 1100 °C’ de a formu ısıtılarak daha yumuşak b formuna dönüştürülür. b formu sıcak sülfürik asit ile reaksiyona sokularak Li2SO4L2So4H5rt5 elde edilir. Elde edilen bu çökelek çözeltiden ayrılarak Na3CO3 ile yıkanır. Böylece suda çözünmeyen LiCO3 elde edilir. Manik depresif tedavisinde ve pillerde kullanılır.
Li2SO3 + Na2CO3 → Na2SO4 + Li2CO3 (katı)
Elde edilen Li2CO3 çökeleği HCl ile reaksiyona sokularak LiCl elde edilir.
Li2CO3 + 2 HCl → 2 LiCl + CO2 + H2O
LiCl erime noktası 600 °C den fazla olduğu için elektroliz ile saflaştırılması zor olduğundan LiCl (55%) ve KCl (45%) karışımı kullanılarak erime noktası 430 °C’ye düşürülür. Bu karışımın elektrolizi ile Li saf olarak elde edilir.
- Katot: Li+ (s) + e- → Li (s)
- Anot: Cl- (s) → ½ Cl2 (g) + e-
İçme Suyunda Lityum ve İlgili Bulgular
1990 yılında, ABD'nin Texas eyaletinin 28 idari bölümünde (county) içme sularındaki lityum miktarı üzerine bir araştırma yayımlanmıştır. Bu araştırma, içme suyundaki lityum miktarıyla intihar, cinayet ve tecavüz vakalarının negatif korelasyon gösterdiğini destekler veriler sunmuştur. Çalışmaya dahil edilen zaman aralığında, suyundaki lityum miktarı en yüksek bölgelerde, en düşük olan bölgelere kıyasla %40 daha az intihar vakası görülmüştür.
2009 yılında Japonya'da, 1 milyon insanın yaşadığı 18 şehri ve 5 senelik bir zaman dilimini kapsayan bir araştırma bu sonuçları desteklemiş. Bunu takiple Avustralya ve Yunanistan'da da bu iddiaları destekler sonuçların elde edildiği araştırmalar yapılmıştır. Bu araştırmanın sahibi araştırmacılar, çok düşük miktarlarda lityuma maruz kalmanın sinir sistemini koruyucu, hatta sinir hücresi gelişimini destekleyici etkilerinin olabileceği fikrini öne sürmüşlerdir.
Bu araştırmada kullanılan verilerin tekrar analiziyle yayımlanan ikinci bir araştırmada, içme suyundaki lityum miktarındaki artışın, çalışmada gözlenen ölüm oranlarıyla negatif korelasyon gösterdiği bulgulanmıştır.
Bu süreçte, İngiltere'de yapılan bir araştırma, yukarıda anlatılanlara aykırı bir sonuç vermiştir. Fakat bu araştırmaya konu olan bölgede içme sularındaki lityum miktarının, öteki çalışmalara ve ilgili bölgelere kıyasla çok daha düşüktür.
Lityumun Kullanım Alanları
İçecek Endüstrisi
"7-Up", piyasaya "Bib-label Lithiated Lemon-Lime Soda" ismiyle sürülmüştür. İçecek, 1950 yılına kadar da lityum sitrat içermiştir. Şehir efsanelerine göre içeceğin ismindeki "7", lityumun atom ağırlığından kaynaklıdır.
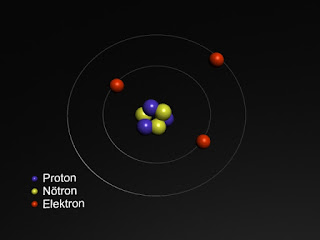 |
| Lityum atomu modeli |
Tıp
Lityum tuzları bipolar bozukluk tedavisinde, duygudurum dengeleyici olarak kullanılmaktadır. Lityumun bu etkisi 1949 yılında Avustralyalı psikiyatr John Cade tarafından belgelenmiştir. FDA, 1970 yılında lityumun etkili bir ilaç olarak tanındığını duyurmuştur.
Lityumun hem depresyon hem mani üzerinde etkisi olsa da manik dönem üzerindeki etkisi daha belirgindir. Lityum, depresyon tedavisinde öteki antidepresanların etkisini güçlendirmek için de kullanılmaktadır.
Lityum, sindirilmesinin ardından, merkezi sinir sisteminde hızla yayılır ve çeşitli nörotransmitterler ve almaçlarla etkileşir. Norepinefrin salınımını azalttığı ve serotonin sentezini arttırdığı bilinmektedir. Mani üzerindeki etkisini ortaya çıkaran mekanizma bilinmemektedir.
Etiketler:
Ansiklopedi
Kelime Etimolojisi (Kökeni) Sözlüğü
Kimya Terimleri Sözlüğü
Türkçe Sözlük
Türkçe'deki Fransızca Kökenli Kelimeler